L'avenir de la recherche
L'hétérogénéité de la maladie et de la réponse aux traitements est un véritable défi pour les scientifiques. Leurs pistes d'études sont multiples et les nombreux essais cliniques en cours témoignent du dynamisme de la recherche. Les tumeurs sont différentes, ce qui rend difficile la prise en charge et induit une réponse au traitement très variable d'un patient à l'autre.
Ainsi, les chercheurs tentent de comprendre les mécanismes moléculaires impliqués dans l'apparition et la progression du cancer pour établir un traitement à la carte en fonction de la génétique de la tumeur. Par ailleurs, certains essais cliniques visent à améliorer l’immunothérapie.
Les recherches actuelles suivent également d’autres directions, comme celle du dépistage. Enfin, le pronostic devrait bénéficier de la recherche de bio-marqueurs, facteurs prédictifs de la réponse au traitement.I. L’immunothérapie
Améliorer l’immunothérapie vise à accomplir des associations médicamenteuses existantes ou à en découvrir de nouvelles pour obtenir une efficacité optimale, ou encore à stimuler les défenses immunitaires du patient pour accroître la lutte contre les cellules cancéreuses.
Une des principaux avantages de l’immunothérapie tient à son efficacité potentielle sur un grand nombre de patients atteints d’une tumeur broncho-pulmonaire. Jusqu’à présent, les grandes avancées thérapeutiques étaient réservées à une petite proportion de malades, comme celles des non-fumeurs pour les thérapies ciblées. À l’inverse, l’immunothérapie concerne plutôt la population des fumeurs, qui représentent 80 % des patients atteints d’un cancer du poumon.
L’immunothérapie fait également l’objet d’essais cliniques dans les formes cette fois localisées donc sans métastase mais non opérables de cancer du poumon, soit environ 15 % des patients. Un essai thérapeutique récent a démontré que chez ces patients, après la radio-chimiothérapie, le durvalumab, une nouvelle molécule d’immunothérapie, triple la durée de survie sans progression de la maladie en comparaison du placebo.
A. Interview de Virginie Westeel pneumo-oncologue:
Le prix Nobel de "physiologie ou médecine" a été remis le lundi 1er octobre 2018 à l'Américain James P. Allison et le Japonais Tasuku Honjo pour leur travaux sur l'immunothérapie. Une technique révolutionnaire, comme nous l'avait expliqué en avril 2016 Virginie Westeel, pneumo-oncologue au CHRU de Besançon et à l'Institut régional fédératif du cancer de Franche-Comté:


- Qu'est-ce que l'immunothérapie appliquée au cancer ?
Virginie Westeel: "Si le cancer du poumon a pu se développer, c'est parce que les cellules cancéreuses ont trouvé le moyen d'endormir l'immunité du patient. L'immunothérapie va donc "réveiller" le système immunitaire pour qu'il reconnaisse à nouveau les cellules tumorales à combattre. C'est une révolution dans nos pratiques".
- Comment fonctionne-t-elle ?
Virginie Westeel: "Les cellules tumorales expriment à leur surface des récepteurs (PDL1), et les lymphocytes T en expriment d'autres (PD1). Leur interaction inhibe les défenses antitumorales de l'organisme. C'est la récente découverte d'anticorps monoclonaux appelés anti-PD1/PD-L1 ou "inhibiteurs de check-point de l'immunité" qui a permis l'essor des immunothérapies pour certains types de tumeurs, en particulier le cancer du poumon. Donnés au patient par perfusion, les anti-PD1/PD-L1 bloquent ces récepteurs tumoraux, permettant ainsi de rétablir la réaction immunitaire contre les cellules cancéreuses."
- Quels sont les traitements en développement ?
Virginie Westeel: "L'immunothérapie ouvre de nombreuses possibilités. Au CHRU de Besançon, nous travaillons sur un vaccin thérapeutique qui sera testé chez l'homme à partir du printemps 2016. Le principe est d'injecter au patient un antigène qui va, là aussi, entraîner une stimulation de la réponse immunitaire antitumorale. Par ailleurs, des essais de traitement de première ligne, donnés en première intention, sont en cours pour les CNPC, ainsi que des traitements pour le cancer du poumon à petites cellules. On cherche également à mieux définir quels patients tirent le plus de bénéfice de ces traitements, à cibler d'autres récepteurs que PD1/PD-L1, et à évaluer l'association de plusieurs immunothérapies."
B. L' essaie clinique: STIMULI IFCT 4-12 par le Dr Cécile LE PECHOUX
Des études récentes ont montré des résultats très prometteurs avec l’immunothérapie qui consiste à stimuler les défenses immunitaires pour aider l'organisme à détruire les cellules cancéreuses. L’Ipilimumab est une immunothérapie, il s’agit d’un anticorps monoclonal qui bloque la fixation des antigènes du lymphocyte cytotoxique 4 ses ligands. Ce blocage permet l’activation des lymphocytes T et stimule leur multiplication, ainsi ces lymphocytes T infiltrent la tumeur et peuvent faire régresser la tumeur.
Tous les patients auront donc le traitement habituel dit « standard ». Dans cette étude, celui-ci repose sur une chimiothérapie de 4 cycles toutes les 3 semaines et des séances quotidiennes de radiothérapie centrée sur la tumeur et les ganglions du médiastin envahis par la tumeur. Les séances de radiothérapie ont lieu 5 jours par semaine, pendant 5 a 6 semaines. Cette radiothérapie commencera en même temps que le deuxième cycle de chimiotherapie. A la fin du traitement, il leur sera proposé un tirage au sort. La moitié des patients n’auront plus de traitement. Les autres patients auront une immunothérapie par Ipilimumab pendant une durée de 2 ans.
L’objectif de cette étude randomisée est de voir si une immunothérapie de consolidation après le traitement standard permet d’améliorer les résultats. Les effets secondaires seront évidemment bien évalués également.
C. Association d’une immunothérapie à la chimiothérapie avec l'essaie clinique KEYNOTE -189
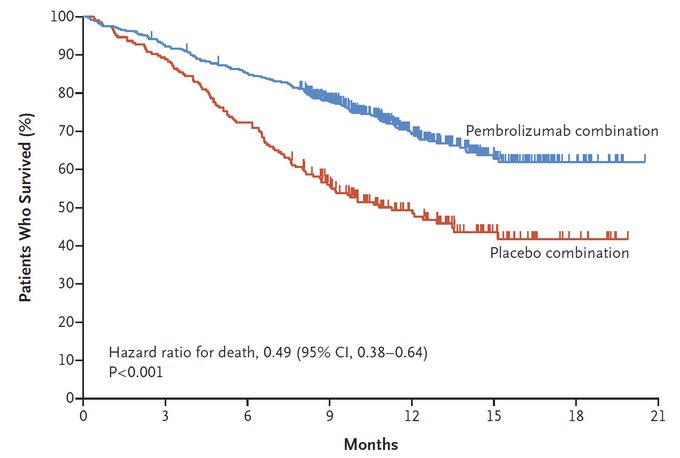
KEYNOTE -189 est un essai contrôlé avec une évaluation indépendante, qui a comparé le pembrolizumab, un anticorps anti-PD-L1, au placebo, en plus d’une chimiothérapie standard (pemetrexed et cisplatine ou carboplatine). Celui ci a etait realise sur sur 616 malades,qui avaient un cancer bronchique non à petites cellules, métastatique, et sans mutation. Il confirme des résultats d’autres immunothérapies dans des études précédentes, à savoir des taux de réponse des cancers de près de 70% lorsqu’elle est associée à la chimiothérapie de référence, versus 50% avec la chimiothérapie seule.
Au terme d’un suivi de 12 mois, la survie globale est de 69,2% chez les patients du groupe immunothérapie (pembrolizumab) versus 49,4% dans le groupe placebo. La survie sans progression de la maladie est également en faveur de l’immunothérapie avec 8,8 mois et de 4,9 mois dans le groupe placebo.
Ces résultats montrent qu’il y aurait intérêt de l’association immunothérapie et chimiothérapie dans le cancer du poumon, l’hypothèse est qu’une partie des cellules cancéreuses sont détruites par la chimiothérapie ce qui active le système immunitaire rend la tumeur plus visible pour lui.
II. Le dépistage
A. Dépistage par scanner systématique
Des experts estiment que la mise en place d’un dépistage par scanner systématique du cancer du poumon chez les gros fumeurs permettrait de sauver environ 7 500 vies par an. Ce dépistage diminuerait la mortalité par cancer du poumon chez les hommes et chez les femmes.
"Si on veut donner un chiffre simple, trois quarts des cancers du poumon sont découverts à un stade tardif actuellement, on ne peut plus les opérer, il est trop tard",
"Quand on dépiste par scanner le chiffre est exactement inverse: trois quarts des cancers sont découverts à un stade précoce, qu'on peut opérer, et donc guérir. (…) Donc on inverse complètement la proportion par un examen qui ne fait pas mal, qui n'est pas toxique, qui est un simple scanner du thorax".
« En faisant passer un simple scanner aux gros fumeurs, on pourrait sauver des milliers de vies chaque année » a expliqué Charles Marquette, chef du service de pneumologie du CHU de Nice. Celui-ci fait partie d’une trentaine d’experts qui réclament la mise en place d’un dépistage systématique du cancer du poumon chez les fumeurs à partir de 50 ans.
Selon une étude présentée en septembre à Toronto au Canada, le dépistage par scanner thoracique réduit la mortalité par cancer du poumon de 25 % chez les hommes et de 40 à 60 % chez les femmes. La Haute Autorité de santé avait pourtant refusé ce dépistage en 2016, invoquant les dangers des rayons et un risque non négligeable de faux diagnostics.
Si la mesure était adoptée en France, sur les personnes âgées de plus de 50 ans et qui fument depuis au moins 25 ans, pas moins de 7.500 vies pourraient être sauvées chaque année.
B. Un « nez électronique »
Le dépistage à pour objectif la mise au point de techniques plus sensibles. Par exemple, un « nez électronique » est actuellement à l’essai : cette technique ultrasensible pourrait être capable d’identifier, grâce à l’air expiré par les patients, ceux qui sont atteints de cancer du poumon.
L’équipe de Hossam Haick, du Technion de Haïfa, en Israël, a développé un nez électronique à base de nanoparticules d’or qui pourrait servir de test diagnostique du cancer du poumon. Ce nanocapteur détecte dans l’air expiré des quantités infimes de petites molécules carbonées, les composés organiques volatils, dont la quantité change chez les personnes souffrant de ce cancer.


La cancérogenèse c’est le cas aussi d’autres pathologies s’accompagne d’un métabolisme qui dégradent les acides gras des membranes cellulaires (peroxydation). Cette dégradation donne naissance à des alcanes, tels l’éthane et le pentane, qui sont excrétés sous forme volatile dans l’air expiré ou encore dans la sueur et l'urine.
H. Haick et ses collègues ont évalué un système miniaturisé et ultrasensible de diagnostic du cancer pulmonaire. Ils ont tout d’abord prélevé de l’air expiré de 40 malades à un stade avancé du cancer et de 56 volontaires en bonne santé. Pour éviter toute contamination extérieure, les participants ont respiré quelques minutes à travers un filtre qui retenait les composés organiques de l'air. De là, les chercheurs ont mis en évidence 42 molécules représentant des bio-marqueurs du cancer du poumon : ils apparaissaient en effet chez au moins 83 pour cent des patients, mais chez moins de personnes en bonne santé, et leur abondance dans l’haleine était modifiée. Neuf nouveaux composés organiques volatils jusqu’alors jamais identifiés dans de l’air expiré et spécifiques des patients, tels le méthyl-octane et le diméthyl-hexane ont était mis en évidence
Les chercheurs ont ensuite conçu une matrice de nanocapteurs capables de réagir aux 42 bio-marqueurs mis en évidence, avec une limite de détection de 1 à 5 micromètres par litre d’air. Ces capteurs comprennent des nanoparticules d’or fonctionnalisées, c’est-à-dire sur lesquelles se greffent naturellement différents groupements chimiques qui peuvent réagir avec des composés organiques volatils . Lorsque des composés volatils s’y fixent, la résistance électrique du capteur est modifiée, formant une signature unique selon la combinaison de composés ainsi détectés.
Ce nez électronique serait-il applicable au diagnostic précoce du cancer du poumon ? Les résultats du groupe israélien ne suffisent pas pour l'affirmer, les malades ayant participé à l’étude étant en phase avancée du cancer ; seuls des essais cliniques le confirmeraient.
C. Recherche de bio-marqueurs, facteurs prédictifs
Chaque tumeur possède une signature moléculaire qui lui est propre. Ainsi, à l’avenir, l’analyse moléculaire des tumeurs guidera le choix du traitement pour chaque malade. En effet, déterminer des facteurs prédictifs de réponse permettra de cibler les patients pour lesquels les traitements disponibles seront les plus efficaces. Identifier et valider des biomarqueurs prédictifs de la réponse aux traitements qui soient pertinents en clinique reste toutefois un véritable défi scientifique. Cette approche a déjà été validée pour certains cancers comme le cancer du sein et le cancer colorectal où des bio-marqueurs ont été identifiés et des tests de diagnostic moléculaire développés et validés.
Dans le cancer du poumon, cet espoir est devenu une réalité avec le projet ERMETIC, initié par l'INC en 2005 et coordonné par l'Intergroupe Francophone de Cancérologie Thoracique, l'Assistance Publique-Hôpitaux de Paris et l'Institut Gustave Roussy avait pour objectif de valider plusieurs techniques de détection des anomalies moléculaires du récepteur de EGFR incluant les mutations de ce récepteur. Le projet a duré plus de 2 ans et a mobilisé une quinzaine d'équipes multidisciplinaires.
Le réseau français de recherche Roche est partenaire de l'IFCT pour le projet ERME TIC-2 qui prolonge le projet ERMETIC. Pour améliorer le dépistage des anomalies de l'EGFR, ERMETIC-2 va évaluer des techniques alternatives, potentiellement plus simples, plus sensibles et moins coûteuses qui ont été utilisées et validées au cours d'ERMETIC. Ces travaux préfigurent l'arrivée d'une médecine personnalisée dans le cancer du poumon.